
© Depositphotos / Evgeny Atamanenko
За эти деньги обещают омолодить организм на 25 лет. По словам врачей, двум пациентам — 79 и 90 лет — в ближайшие дни сделают первые инъекции. Ранее о подобной процедуре сообщила генетик Элизабет Периш. Правда, ее данные многие ученые считают сомнительными. РИА Новости разбирается, на чем основаны новые методы омоложения и насколько они эффективны.
Заставить клетки делиться вечно
В 2012 году испанские исследователи показали, что генная терапия способна продлевать жизнь — в частности, лабораторным мышам. Взрослым (12 месяцев) и пожилым (24 месяца) грызунам вводили специально созданный вирус с активным геном теломеразы. Вирус внедрял свою ДНК в клетки животных и заставлял их производить этот фермент.Дело в том, что теломераза удлиняет концевые участки хромосом — теломеры, величина которых, по некоторым данным, коррелирует с продолжительностью жизни. В норме при каждом делении клетки теломеры уменьшаются и когда они становятся критически короткими, клетки уже не могут делиться и чинить повреждения в тканях. В результате организм стареет. Исключение — половые и стволовые клетки, размножающиеся намного дольше — как раз благодаря теломеразе.
© Depositphotos / edesignua
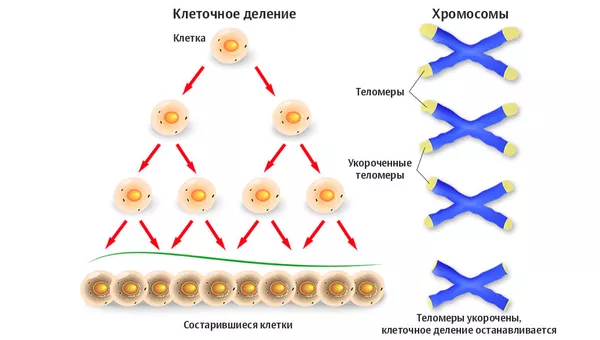
При делении клеток теломеры, расположенные на концах хромосом, не допускают их слипания и латают те участки молекулы ДНК, которые недокопировались в процессе деления. С каждым делением теломеры укорачиваются. Когда они израсходованы, клетки не могут размножаться. Укорочение теломер считается одной из основных причин клеточного старения.
Испанские генетики предположили, что благодаря ферменту мыши проживут дольше. Так и получилось: продолжительность жизни годовалых грызунов, которым вводили активный ген теломеразы, в среднем увеличилась на 24 процента. Их двухлетние сородичи после генной терапии жили на 13 процентов дольше ровесников из контрольной группы. При этом у животных, получивших активный ген теломеразы, улучшилась нейромускулярная координация и замедлилось развитие остеопороза. Оба показателя считаются маркерами старения.
Кроме того, у подопытных мышей не возникло онкологических заболеваний, хотя считается, что за "бессмертие" раковых клеток тоже несет ответственность теломераза.
© 2012 EMBO Molecular Medicine
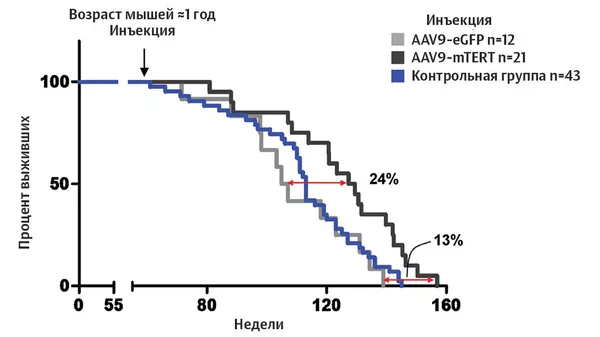
График, показывающий, насколько увеличилась продолжительность жизни мышей в эксперименте испанских ученых. Черным цветом обозначена группа животных (21 особь), которым вводили вирус (AAV9), содержащий активный ген теломеразы (mTERT). Серым цветом — грызуны (12 особей), получившие вирус (AAV9) с зеленым флуоресцентным белком (eGFP). Он не оказывал никакого влияния на клетки. Синим цветом помечены звери (43 мыши), которым не делали никаких инъекций.
Затормозить старение
Ученые Хьюстонского методистского исследовательского института (США) провели успешные опыты по генной терапии на культурах клеток человека, удлинив теломеры и таким образом затормозив преждевременное старение клеток, взятых у больных прогерией. При этом заболевании нарушается работа гена, отвечающего за производство белка ламина, входящего в оболочку клеточного ядра. ДНК хуже ремонтируется, теломеры быстрее разрушаются, и организм дряхлеет. Пациенты с таким диагнозом живут в среднем не больше 13 лет.У больных взяли образцы фибробластов — клеток соединительной ткани — с укороченными теломерами. А затем трижды с интервалом в 48 часов вводили в них матричную РНК, кодирующую человеческую теломеразу. В результате фибробласты продолжали делиться, преждевременное клеточное старение замедлилось. При этом ученые заметили, что фибробласты омолаживаются — теломераза в них стала активнее и теломеры длиннее.
Проверить на человеке
В сентябре 2015 года генетику Элизабет Пэриш, возглавляющей стартап BioViva (США), внутривенно ввели генетические конструкции, активирующие теломеразу и стимулирующие синтез фоллистатина — белка, влияющего на мышечный рост. Это произошло в одной из больниц Колумбии, ее название и имя врача, делавшего инъекции, не разглашают.Три года спустя Пэриш заявила, что ее теломеры значительно удлинились, а организм помолодел на несколько лет. Но она так и не опубликовала результаты этого эксперимента ни в одном рецензируемом научном журнале. Единственный бесспорный итог в том, что исследовательница жива и, судя по анализам, неплохо себя чувствует.
Сейчас опыт Пэриш намерены повторить сотрудники Libella Gene Therapeutics. Они зарегистрировали клиническое испытание генной терапии на официальном американском сайте clinicaltrials.gov. Однако сами исследования собираются проводить в одной из колумбийских больниц, вне юрисдикции американского Минздрава — FDA.
По словам представителей компании, на днях двум пациентам — 79-летнему мужчине и 90-летней женщине — введут генетические конструкции с активным геном теломеразы. Первые результаты обещают сообщить через год.
Научное сообщество относится к этим экспериментам весьма скептически. Во-первых, исследование проводят не в США — это может говорить о том, что его авторы хотят избежать контроля со стороны властей. Во-вторых, согласно последним данным, длина теломер как таковая плохо коррелирует с продолжительностью жизни разных видов млекопитающих. Долголетие скорее зависит от скорости утраты теломер.Поэтому некоторые ученые предлагают включать в генетические конструкции, используемые в подобной терапии, не активный ген теломеразы, а гены, связанные с устойчивостью к возрастным болезням. Например, недавно научная группа Гарвардского университета (США) с помощью коктейля из трех таких генов вылечила престарелых мышей от ожирения, диабета второго типа, почечной и сердечной недостаточности. В итоге грызуны прожили дольше, чем животные из контрольной группы.
ria.ru


