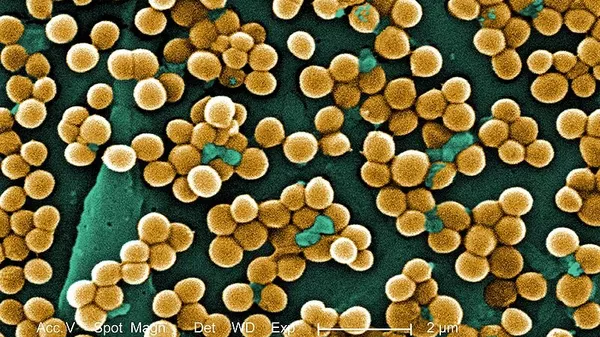
© Фото : Janice Haney Carr, Centers for Disease Control and Prevention
Золотистый стафилококк
Результаты исследований опубликованы в журнале Nature Communications.
Работа стала результатом пятилетнего сотрудничества между Казанским федеральным университетом (КФУ), Институтом белка РАН, Штутгартского университета в Германии и Института генетики и молекулярной и клеточной биологии в Страсбурге (Франция). В 2016 году команда первой полностью описала структуру рибосомы Staphylococcus aureus и сравнила ее с другими организмами. Сейчас же учеными раскрыт один из механизмов стрессоустойчивости этих опасных бактерий, что, по мнению авторов, будет способствовать поиску новых эффективных антибиотиков.
"Рибосома — это самый большой рибонуклеиновый комплекс в клетке, и он состоит из двух субъединиц: большой и малой. Малая субъединица отвечает за прочтение генетического кода, а функция большой субъединицы заключается в обеспечении протекания реакции образования пептидной связи в растущей цепи белка", — приводятся в пресс-релизе КФУ слова одного из авторов исследования Константина Усачева, руководитель Лаборатории структурной биологии Института фундаментальной медицины и биологии КФУ, доцент кафедры медицинской физики Института физики КФУ.
Ученые описали механизм выживания клеток бактерий во время стресса, когда они переходят в режим энергосбережения, чтобы переждать неблагоприятные условия.
"В нашей статье с помощью методов криоэлектронной микроскопии и рентгеноструктурного анализа мы смогли показать механизм связывания с рибосомой белка RsfS (Ribosome silencing factor S), который защищает золотистый стафилококк от стрессов — антибиотиков, повышенной температуры, иммунитета хозяина", — говорит Усачев.
Долгое время исследователям не удавалось получить в высоком разрешении структуру комплекса бактериальных рибосом с белком RsfS, чтобы понять детали механизма его действия. Одной из проблем была высокая токсичность данного белка для клеток бактерий кишечной палочки E.coli — организма, используемого для получения белков в лабораторных условиях.
"Дело в том, что RsfS, останавливающий синтез белков у золотистого стафилококка, способен останавливать этот процесс и у других бактерий. Это приводило к получению очень малого количества образца белка, недостаточного для проведения структурных исследований, — рассказывает ученый. — Тогда нам пришла идея выделить данный белок одновременно с его мишенью в структуре рибосомы стафилококка – белком L14, входящим в состав большой субъединицы. Выяснилось, что если выделять обе компоненты одновременно, то ни будут стабильными в растворе. Нам удалось получить кристаллы этих белков и решить структуру методом рентгеноструктурного анализа сначала со средним разрешением с помощью имеющегося в нашей лаборатории нового монокристального дифрактометра, а затем с высоким разрешением — на синхротроне ESRF в Гренобле во Франции".
Далее ученым потребовалось изучить детали процесса взаимодействия белка RsfS с рибосомой золотистого стафилококка, что было сделано с помощью метода криоэлектронной микроскопии.
"К сожалению, микроскопа, позволяющего решать структуры с высоким разрешением этим методом, в нашем распоряжении не было, но тут нашими исследованиями заинтересовалась французская фармацевтическая компания NovAliX и предложила свой микроскоп для тестирования начальных образцов", — поясняет Усачев.
В результате, комбинируя данные криоэлектронной микроскопии с полученными ранее данными рентгеноструктурного анализа, авторам удалось детально показать молекулярный механизм действия белка RsfS на рибосомы золотистого стафилококка.
Сейчас ученые заняты поиском и изучением белков, управляющих работой рибосомы патогена. Для этого они используют методы генетики, биохимии, молекулярной биологии и биофизики. По словам исследователей, это необходимо, чтобы создать фармацевтические препараты, которые смогут победить штаммы патогенных бактерий, в том числе золотистый стафилококк, устойчивые ко всем существующим на данный момент антибиотикам.
ria.ru


