Точная доставка лекарств или инструментов для терапии к больным тканям значительно повышает эффективность лечения при одновременном снижении побочных эффектов, а также позволяет вводить препарат в организм в гораздо меньшем количестве. Исследователи из Медицинской школы Калифорнийского университета в Сан-Диего и Онкологического центра Мурса в Калифорнийском университете в Сан-Диего создали безопасное средство доставки лекарств к тканям-мишеням. Для этого они генетически модифицировали мезенхимальные стволовые клетки (МСК) таким образом, чтобы они содержали рецепторы-хемоаттрактанты (для перемещения по градиенту концентрации) и молекулы, связывающие эндотелиальные клетки, а затем методом центрифугирования удалили из них ядра, сохранив органеллы, которые производят энергию и белки, необходимые для выполнения жизненных функций.
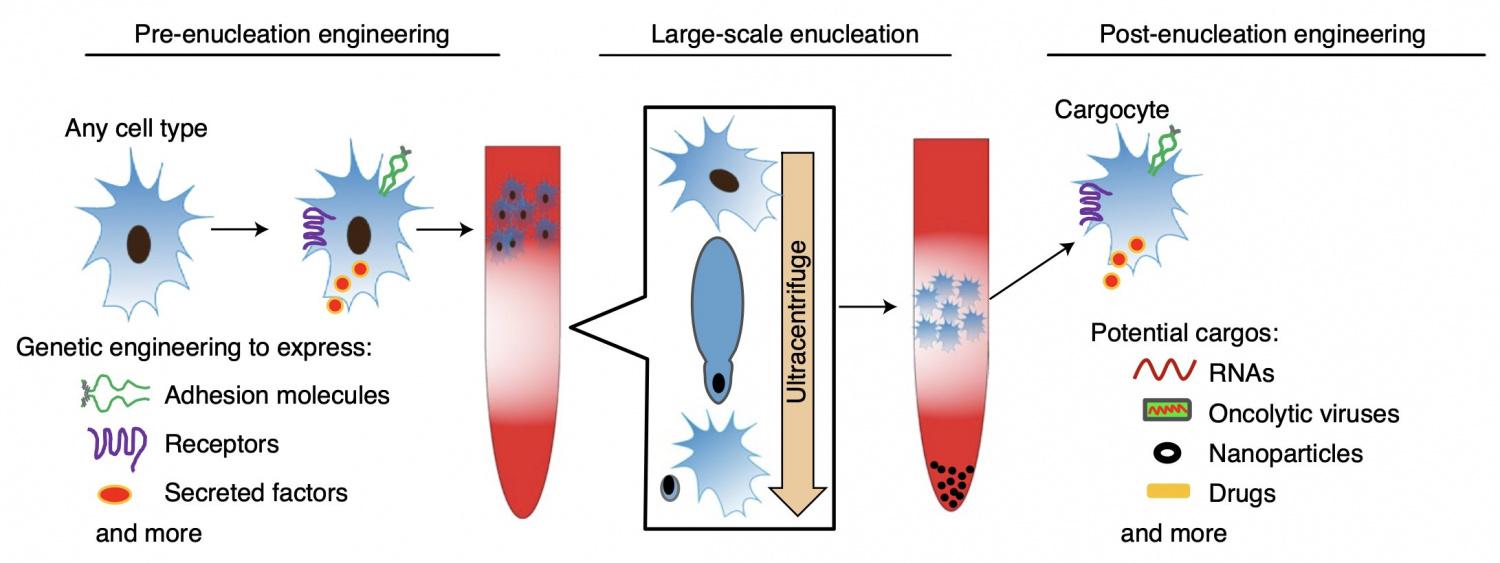
Чтобы проверить качество доставки безъядерными клетками, группа, возглавляемая Ричардом Клемке, создала так называемые каргоциты (от англ. «cargo» – груз), наполнила их противовоспалительными цитокинами и ввела мышиным моделям острого воспаления и панкреатита. В течение нескольких дней цитокины накапливались в тканях-мишенях, где изменяли иммунный ответ и уменьшали активность воспаления, что сопровождалось облегчением течения заболевания.
Исследователи обнаружили, что каргоциты сохраняли способность осуществлять большую часть своих клеточных функций, но также обладали способностью безопасно переносить и доставлять терапевтические препараты конкретно в целевые ткани. Это открывает возможность лечения заболеваний путем доставки лекарств именно туда, где они необходимы, с меньшей вероятностью нежелательных побочных эффектов, связанных с тем, что эти лекарства поступают в другое место.
Авторы заявили, что использование энуклеированных (лишенных ядер) модифицированных МСК имеет ряд преимуществ по сравнению с подходами, в которых в качестве средств доставки используются полноценные клетки.
Во-первых, получить одобрение регулирующих органов на клиническое использование значительно измененных стволовых клеток, которые обладают способностью к пролиферации и дифференцировке, трудно из соображений безопасности.
Во-вторых, первичные клетки, взятые у доноров для целей терапевтической доставки, обладают ограниченными биоинженерными и терапевтическими возможностями.
В-третьих, каргоциты имеют более определенную и предсказуемую судьбу после введения в организм: они не могут осуществлять транскрипцию и продуцировать нежелательные факторы, дифференцироваться в нежелательные типы клеток или приживаться в тканях с нежелательными последствиями.
Следующие шаги Клемке и его коллег включают создание каргоцитов, способных доставлять множество различных терапевтических средств в больные ткани in vivo, изучение возможностей для создания и энуклеации других типов клеток, включая иммунные клетки, и разработку аналогичного подхода для поиска и уничтожения метастатических онкологических заболеваний.
Статья H.Wang et al. Genetically engineered and enucleated human mesenchymal stromal cells for the targeted delivery of therapeutics to diseased tissue опубликована в журнале Nature Biomedical Engineering:
Аминат Аджиева, портал «Вечная молодость» vechnayamolodost.ru по материалам UC San Diego: Nuclei-free Cells Prove Utility in Delivering Therapeutics to Diseased Tissues.


